Zvykli sme si na to, že ľudia sa často snažia určiť jednu konkrétnu živinu a nájsť k nej mechanizmus, čo následne prepoja s konkrétnou chorobou. To by sa však dalo prakticky urobiť s akoukoľvek živinou. Preto je vždy dôležité pozrieť sa na danú problematiku cez tzv. "body of evidence", teda súhrn dôkazov, ktoré vyplývajú z odbornej literatúry a vedeckých štúdií. A presne o to sme sa pokúsili v sérii nasledujúcich článkov, ktoré prinesieme. V tejto trojsérii sa zameriame na to, akú úlohu zohráva príjem cholesterolu, nasýtených tukov a ďalších zložiek stravy v kontexte rozvoja srdcovo-cievnych ochorení, predovšetkým aterosklerózy. Uvedomujeme si, že ide o veľmi obsiahlu a ťažkú tému, no posnažíme sa vždy náročné pasáže pre pochopenie čo najviac preložiť do "ľudskej reči".
Špeciálny kredit patrí dvojici Danny Lenon a Alan Flanagan, ktorí v rámci Sigmanutrition poskytli absolútne skvele spracovaný základ pre túto sériu, ktorý sme rozšírili a vhodne doplnili.
Akú úlohu zohrávajú lipidy, cholesterol a lipoproteíny pri ateroskleróze a rozvoji srdcovo cievnych ochorení (CVD)?
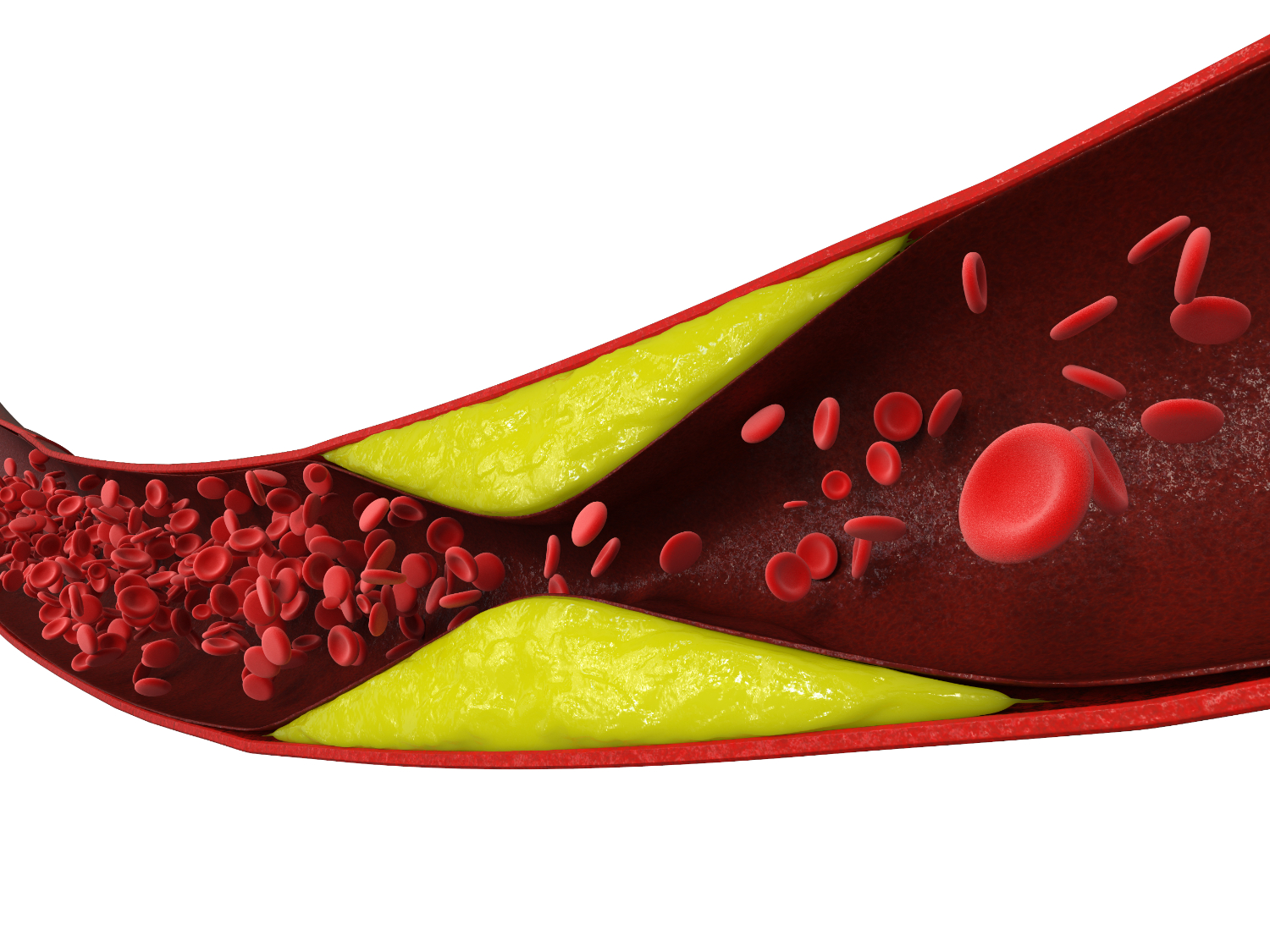
Ateroskleróza predstavuje ochorenie tepien, pri ktorom sa do poškodenej cievnej steny ukladajú tukové látky, najmä cholesterol. Priechodnosť artérie (tepny) sa tým zužuje, čo obmedzuje prietok krvi. Vývoj aterosklerózy vyžaduje, aby častice nesúce lipidy (tzv. lipoproteíny) prenikli arteriálnou stenou (stenou tepny). To umožňuje usadeninám lipidov, cholesterolu a iných látok tvoriť povlak, tzv. plak (ten môže byť pevný - kalciový, ale aj "mäkký"). Ateroskleróza môže byť predchodcom kardiovaskulárnych príhod a spadá pod skupinu srdcovo-cievnych ochorení.
ℹ️ Dôvod, prečo sa ateroskleróza nevyvinie v našich žilách v porovnaní s tepnami, je ten, že tepny sú oveľa viac vysokotlakovým systémom, čo zvyšuje ukladanie spomenutého plaku. Žily teda nemajú dostatočne vysoký tlak, aby spôsobili takéto usadzovanie.

"Krvné lipidy“ predstavujú široký pojem pre rôzne druhy lipidov, ktoré cirkulujú v krvnom riečisku, buď ako voľné (neviazané) molekuly, alebo sa viažu na iné štruktúry. Pretože lipidy sú hydrofóbne (nie sú rozpustné vo vode), aby sa mohli prenášať krvou, potrebujú na svoj transport byť v štruktúrach, ktoré pôsobia ako „nosiče“. Tieto štruktúry, ktoré prenášajú tuky a cholesterol v tele, sú známe ako lipoproteíny. Lipoproteínové štruktúry zahŕňajú fosfolipidy, voľný cholesterol a proteíny nazývané apolipoproteíny.
ℹ️ Ateroskleróza je ochorenie tepien, pri ktorom sa v dôsledku vysokého tlaku v arteriálnom systéme ukladá cholesterol a lipidy do steny tepny, čím sa tvorí tzv. plak, ktorý zužuje priechodnosť ciev a tak zvyšuje riziko kardiovaskulárnych ochorení (KVO).
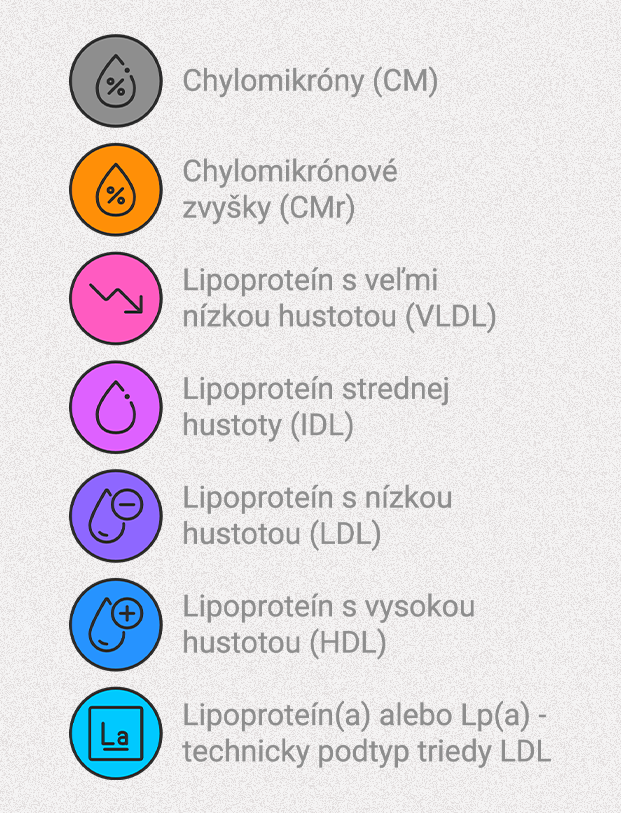
Lipoproteíny rozdeľujeme do niekoľkých kategórií, ktoré sú klasifikované podľa ich veľkosti a hustoty:
„Hustota“ v tomto kontexte predstavuje množstvo lipidov v pomere k množstvu obsiahnutých proteínov (apolipoproteín) v danej častici. Takže viac lipidu a menej proteínu znamená väčšiu a menej hustú časticu. Pričom menej lipidov a viac proteínu znamená síce menšiu ale zato hustejšiu časticu.
Napríklad zloženie VLDL je zhruba 92 % lipidov a 8 % proteínov; pretože lipidy sú veľké zlúčeniny, znamená to, že VLDL sú veľké lipoproteíny s nízkou hustotou. Naopak, zloženie HDL je približne 58% lipidov a 42% proteínov; toto zloženie s vysokým obsahom bielkovín spôsobuje, že HDL je „hustý“ a zároveň najmenší zo všetkých podtried lipoproteínov. Pozri na grafické vyobrazenie jednotlivých častíc nižšie, pretože táto informácia bude dôležitá pri určení, ktoré lipoproteíny sú aterogenné a ktoré zase nie.
- Zvýšená hustota = zvýšený obsah proteínov a znížený obsah lipidov
- Znížená hustota = znížený obsah proteínov a zvýšený obsah lipidov
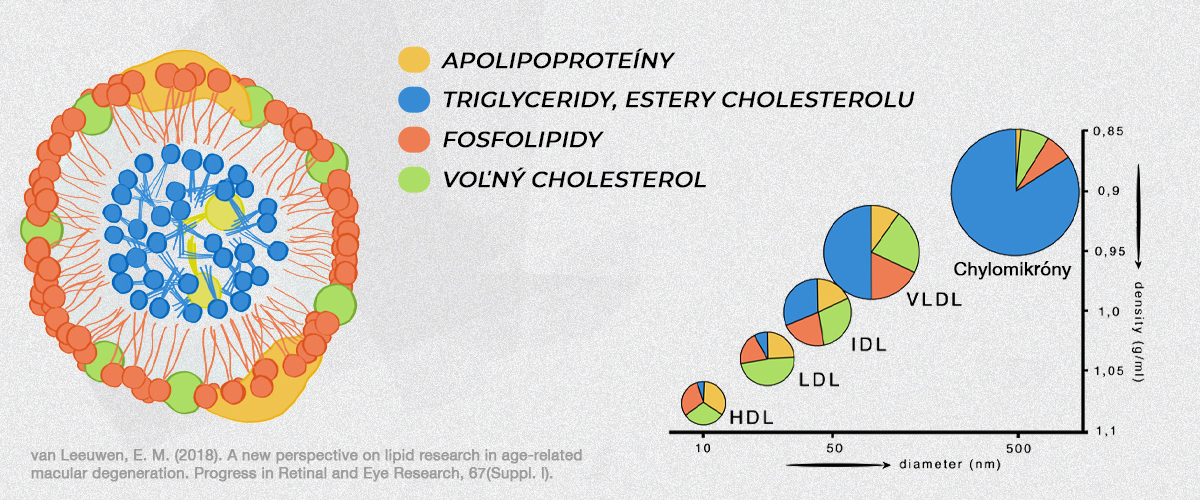
Hlavnou formou tuku prijímaného potravou je triglycerid (TG), ktorý sa skladá z troch mastných kyselín a chrbtice cukrového alkoholu, známeho ako glycerol. Triglyceridy a cholesterol z potravy (hoci menšie množstvá) sa absorbujú do enterocytov (črevné bunky) a balia sa do chylomikrónov (to sú tie najväčšie nosiče, viď vyššie). Takto sa lipidy dostávajú do obehu z vonkajších zdrojov potravy (označovaných ako exogénna cesta). Chylomikróny vstupujú do obehu a triglyceridy, ktoré nesú, sú štiepené enzýmom lipoproteín lipázy (LPL) a sú buď použité alebo uložené v tukovom alebo svalovom tkanive. Tento proces znižuje množstvo lipidov prenášaných v chylomikrone. Keď chylomikróny stratia svoj lipidový obsah, zostávajúce zvyšky sa označujú ako „zvyšky chylomikrónu“ (Chylomicron remnants (CMr)), a tie sa absorbujú v pečeni.
Pečeň je miestom „endogénnej/vnútornej dráhy“, čo znamená, že v pečeni sa vytvára VLDL (druhá najväčšia častica, viď vyššie), aby transportoval nové triglyceridy (z cirkulácie voľných mastných kyselín alebo z nadmernej konzumácie jednoduchých cukrov). Rovnako ako chylomikróny, triglyceridy vo VLDL sa štiepia pomocou LPL a využívajú alebo ukladajú v tukových a svalových tkanivách. Ako sa obsah ich lipidov znižuje, VLDL vytvára IDL a proces rozkladu triglyceridov pokračuje do bodu, keď IDL zase vytvára LDL. Pretože tento proces začína v pečeni a má za následok transport lipidov do tkanív a postupný vývoj VLDL na LDL, často sa nazýva „priamy transport cholesterolu“.
Poznáme však aj tzv. „reverzný transport cholesterolu“. Ten sa uskutočňuje pomocou HDL, ktorý sa tvorí v pečeni. HDL zhromažďuje cholesterol, ktorý efluxuje (opúšťa bunku, v ktorej sa využíval) z buniek v tele a môže transportovať cholesterol buď priamo do pečene alebo premeniť na VLDL a chylomikrony.
a) V prípadoch, keď sa prostredníctvom HDL vráti cholesterol priamo do pečene, cholesterol sa transportuje do pečene, kde sa oxiduje a vylučuje žlčou. Keď sa cholesterol doručí do pečene, pečeň odčerpá z HDL častice jej cholesterol a častica sa môže potom vrátiť do obehu, aby pokračovala v zhromažďovaní (exfluovaného) cholesterolu.
b) V druhom prípade môže HDL premeniť cholesterol na VLDL a chylomikróny výmenou za rovnakú hmotnosť triglyceridov. Tento proces je sprostredkovaný transferovým proteínom cholesterolu (CETP). Tieto VLDL a chylomikrónové častice a ich obsah cholesterolu môžu byť potom rýchlo odstránené pečeňou, čím sa z obehu odčerpá prebytočný cholesterol, zatiaľ čo sa HDL zostáva v obehu.
S menej lipidmi vo forme triglyceridov (VLDL→IDL→LDL) sa tieto lipoproteíny vyznačujú tým, že sú obohatené cholesterolom. A práve schopnosť jednotlivých lipoproteínov obohatených cholesterolom preniknúť do tepien je určená predovšetkým ich veľkosťou.
Nižšie môžeš vidieť veľkosti priemeru rôznych tried/kategórii lipoproteínov (nm = nanometre):
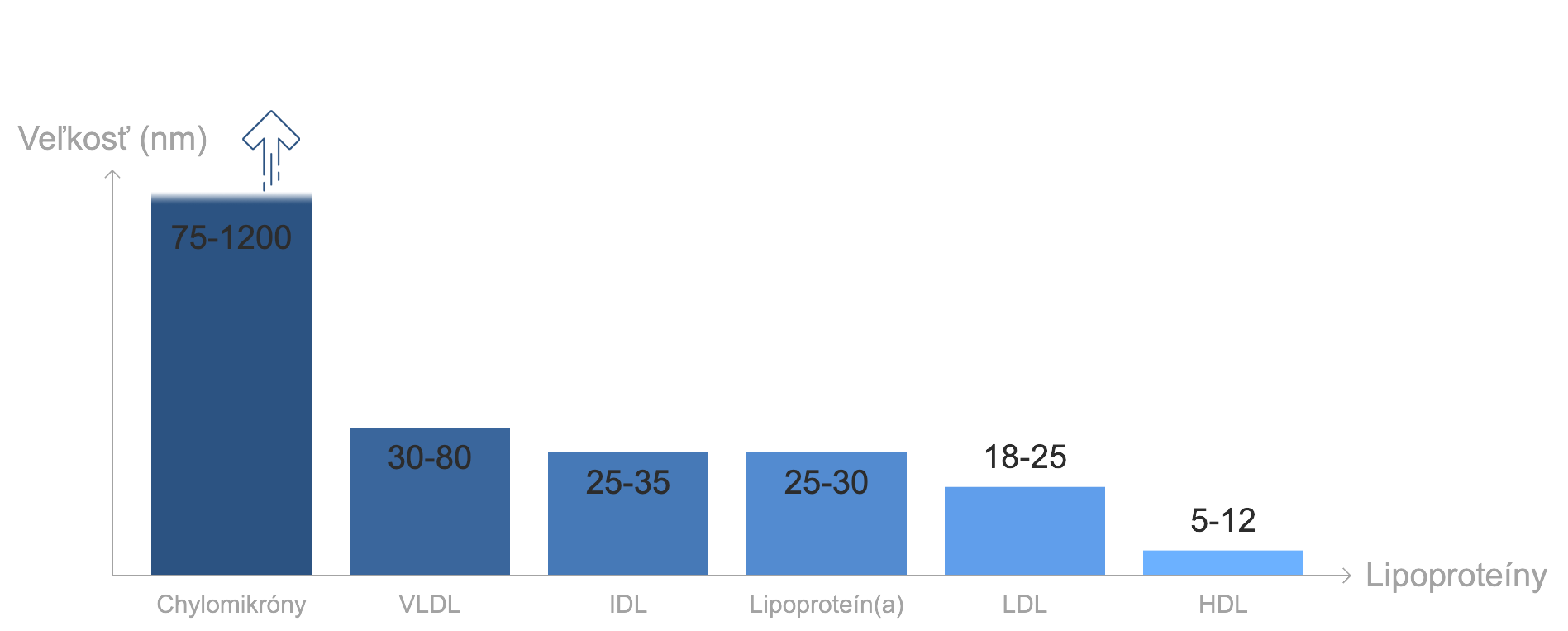
Veľkosť a hustota lipoproteínov je teda rozhodujúca pre schopnosť týchto častíc vstúpiť do tepny. Lipoproteíny s priemerom > 75 nm sú príliš veľké na to, aby prenikli = chylomikróny a veľké častice VLDL teda nie sú aterogénne („aterogénne“ znamenajú schopnosť tvoriť spomenuté plaky v tepnách). Menšie častice, konkrétne: VLDL, IDL, LDL a Lp (a), sú všetky proaterogénne lipoproteíny. A čo spomínaný HDL, ten hovorovo označovaný "dobrý cholesterol"?
ℹ️ Dôvod, prečo je HDL je menej problematický tkvie nielen v jeho veľkosti ale aj v tom, že je to transportér v smere do a nie z pečene (vychytáva cholesterol) a zároveň je aj po kratšiu dobu v obehu.
Vďaka svojej veľmi malej veľkosti a hustote je HDL schopný nielen preniknúť do tepien, avšak ako najmenší lipoproteín má tiež kapacitu z nich aj vystúpiť (pozri obrázok nižšie - cez adventíciu artérie). Takže HDL tam jednoducho neostáva. Naopak, častice VLDL, IDL, LDL a Lp (a) sú všetky dostatočne malé na to, aby jednak prenikli do tepien, ale zároveň sú tak veľké, že sa nemôžu dostať naspäť (viď grafické znázornenie vľavo). Jediným spôsobom, ako je možné tieto lipoproteíny odstrániť zo steny artérie (tepny), je rovnakou cestou akou vstúpili dnu. Avšak tento spätný transport ide proti gradientu krvného tlaku, a preto sa tieto lipoproteíny a ich obsah cholesterolu zachytia v arteriálnej stene. Tým sa iniciuje proces aterosklerózy, tvorby a nahromadenia arteriálneho plaku.

Treba však doplniť, že transcytóza, teda proces prieniku lipoproteínov s nízkou hustotou z lumina (vnútra tepny) do arteriálnej intimy, nie je iba pasívnym prienikom cez poškodený endotel (vnútorná výstelka tepny), ale zároveň ide aj o aktívny proces, ktorého sa zúčastňujú plazmatické receptory na membráne endotélia – scavengerový receptor B1 (SR-B1) a receptor ALK1 (Activin receptor-Like Kinase 1). V preklade do reči ľudskej, aj ľudia bez vysokého krvného tlaku môžu mať pri nesprávnom stravovaní aterosklerózu.
ℹ️ Aterogénne lipoproteíny (VLDL, IDL, LDL a Lp(a)) sú dostatočne malé na preniknutie do steny tepny, avšak príliš veľké na návrat, čím sa zachytávajú a podporujú tvorbu plakov. Na rozdiel od nich HDL, vďaka svojej malej veľkosti a smeru transportu cholesterolu do pečene, nezvyšuje riziko aterosklerózy.
Cholesterol ako pôvodca aterosklerózy
Ak máš po 40tke a čaká ťa preventívna prehliadka u lekára alebo si len chceš pre zaujímavosť skontrolovať svoje aktuálne hladiny cholesterolu v krvi, môžu ťa zaujímať súčasné usmernenia pre hodnoty celkového cholesterolu uvedené nižšie.

Celkový cholesterol
Na úrovni populácie si celkový cholesterol (TC) stále zachováva pozíciu pre klinické a skríningové meranie, ktoré sa má zohľadniť pri dlhodobom hodnotení rizika kardiovaskulárnych ochorení (KVO). Je to odporúčané Európskou spoločnosťou pre aterosklerózu. Pridanie ďalších lipoproteínových častíc však môže zvyšovať presnosť prediktívneho rizika.
Treba však dodať, že kontroverzné je, že vo Framinghamskej kohorte sa až 35% incidencie KVO vyskytlo u subjektov s celkovou hladinou cholesterolu nižšou ako 5,2 mmol / l (<200 mg / dl). To však neznamená, že u väčšiny populácie stále neplatí lineárny vzťah. Riziko exponenciálneho nárastu s nárastom TC existuje, pričom sa zvyšuje štvornásobne z hodnoty 5 mmol / l na 7,8 mmol / l (200 až 300 mg / dl).
Aj pri úrovni TC <5,2 mmol / l (200 mg / l) existuje vysoká pravdepodobnosť, že LDL-C môže byť na úrovni > 3 mmol / l (116 mg / dl). To predstavuje dostatočnú úroveň v priebehu obdobia 20-40 rokov, ktoré prispievajú k ateroskleróze. Ateroskleróza sa môže teda vyvíjať aj na úrovni rozsahu, ktorý je v súčasnosti definovaný ako normálny cholesterol. V tejto súvislosti je zaujímavé podotknúť, že populácie, ktoré stále žijú tradičným životným štýlom „lovcov a zberačov“ často vykazujú hladiny TC <3,1 mmol / l (120 mg / dl) a netrpia týmto problémom.
ℹ️ Celkový cholesterol (TC) zostáva kľúčovým markerom rizika kardiovaskulárnych ochorení, pričom jeho zvýšené hladiny exponenciálne zvyšujú riziko aterosklerózy. Tá sa však môže vyvinúť aj pri hodnotách považovaných za normálne (do 5,2 mmol/l), ak hodnoty LDL-C sú na úrovni > 3 mmol / l.
Chylomikróny a VLDL
Ako už bolo uvedené, veľkosť priemeru chylomikrónov a veľkých VLDL častíc (> 75 nm) má za následok, že tieto lipoproteíny sú príliš veľké na to, aby prenikli do artérií. Lipoproteíny tejto veľkosti teda nie sú samé osebe aterogénne. Avšak progresívne odbúravanie triglyceridov prenášaných týmito lipoproteínmi vytvára „zvyškové lipoproteíny“, ktoré sú už menšími časticami. A tie sú schopné arteriálnej penetrácie. Keďže chylomikróny a veľké VLDL častice obsahujú prevažne triglyceridy (86 % a 55 %), rozklad týchto triglyceridov znižuje veľkosť ich častíc a zvyšuje relatívne zloženie cholesterolu. Tieto chylomikróny obohatené o cholesterol sú proaterogénne, rovnako ako menšie častice VLDL a IDL. Takéto zvyškové častice prevládajú pri kombinovanej hypercholesterolémii, pri ktorej sú zvýšené hladiny celkového cholesterolu a tiež zvýšené triglyceridy v rozsahu 2-10 mmol/l (176-880 mg/dl), čo vedie k zvýšeniu zvyškov chylomikrónov a VLDL bohatých na triglyceridy a IDL. Tento stav sa potom označuje ako hyperlipidémia.
Triglyceridy
Vysoká hladina cirkulujúcich triglyceridov (TGs) sa v minulosti považovala za samostatný rizikový faktor pre KVO. Avšak po úprave na non-HDL-cholesterol (čo je jednoduchý vzorec - celkový cholesterol mínus HDL-C - pričom zostávajúca hodnota predstavuje obsah cholesterolu vo všetkých proaterogénnych lipoproteínoch) sa táto asociácia ukázala ako nulová.
Porovnanie účinku farmakologického zníženia TGs so znížením LDL-C ukázalo, že keď sa hodnotí ako zníženie non-HDL-C, účinok na zníženie kardiovaskulárnych príhod je rovnaký. Zdá sa, že cirkulujúce TGs ako riziko pre KVO môžu byť v skutočnosti čiastočnou náhradou za všetky lipoproteíny bohaté na aterogénne triglyceridy, čo sa dá však odhadnúť aj pomocou hodnoty non-HDL-C. Takže samotné TGs v tomto smere nie sú primárnym problémom pri ateroskleróze.
Toto je dôležité pri častom argumente z rôznych keto a carnivore komunít, ktoré naznačujú, že nízke TGs (<2 mmol / l; 176 mg / dl) znamená, že lipidový profil je „dobrý“, a to aj napriek zvýšenému LDL-C (alebo LDL-P). Je však potrebné zdôrazniť, že zvýšené hladiny aterogénnych lipoproteínov, dokonca aj v kontexte inak nízkeho TG, sú stále dostatočné na vyvolanie aterosklerózy. V tejto súvislosti existuje menší aterogénny príspevok zvyškových lipoproteínov, ale LDL, VLDL a IDL všetky zostávajú proaterogénne.

LDL-C & LDL-P
A tu sa dostávame k laicky známemu "zlému cholesterolu". Aby sme to uviedli na pravú mieru, je dôležité rozlišovať medzi dvoma výrazmi (a značkami), ktoré sa často používajú vzájomne zameniteľne:
- Lipoproteín s nízkou hustotou: označený ako LDL (alebo počet týchto častíc je označený ako LDL-P)
- Lipoproteínový cholesterol s nízkou hustotou: označovaný ako LDL-C
Práve LDL-C sa bežne meria pri štandardnom odbere krvi. Možné je zmerať aj LDL-P (počet LDL častíc). To je však skôr neštandardné a namiesto priameho merania LDL-P je bežnejšie vidieť meranie hladín apolipoproteínu B (ApoB) v plazme používané pre odhad koncentrácie častíc LDL. Keďže apolipoproteín B je apolipoproteín pripojený nielen k LDL, ale aj k chylomikrónom, VLDL a IDL časticiam, meranie ApoB hodnotí celkový počet všetkých týchto (aterogénnych) častíc. Vo väčšine prípadov existuje zhoda medzi LDL-C a ApoB alebo LDL-C a LDL-P (čo znamená, že sa navzájom škálujú; napr. vysoký LDL-C znamená vysoký LDL-P ). U niektorých jednotlivcov však bude medzi týmito meraniami nesúlad, ktorý môže vysvetľovať, prečo údaje konzistentne ukazujú, že ApoB (a LDL-P) je silnejšie spojený s CVD ako LDL-C.
Príčinný vzťah medzi LDL-C a vývojom aterosklerózy bol u ľudí komplexne demonštrovaný mnohými dôkazmi. Týka sa to nielen rozsahu zvýšených LDL-C, ale aj trvania celkovej expozície. Úlohou LDL-C pri riadení aterosklerózy je teda kumulatívna integrovaná expozícia v priebehu života. Táto skutočnosť je dôvodom, prečo je relatívne zníženie rizika zásahov na zníženie hladiny cholesterolu v starších populáciách (70 - 89 rokov) podstatne menšie ako zníženie rizika pri intervenciách v skoršej časti života (40 - 49 rokov). Preto je dôležité, aby si sa o túto problematiku zaujímal už teraz (v 20-40 roku života, nie až v 50tke!).
Existuje aj mylný názor, že aterogénne sú iba menšie a husté častice LDL-C. Toto je však nesprávne chápanie, ktoré neberie do úvahy stupeň obohatenia väčších alebo menších častíc LDL-C cholesterolom. Ak sa v arteriálnej stene zachytí väčší počet menších častíc, vzhľadom na ich nižší obsah cholesterolu na časticu, je množstvo uloženého cholesterolu podobné menšiemu počtu väčších častíc s vyšším obsahom cholesterolu na časticu. Nakoniec sú všetky častice LDL-C rovnako aterogénne bez ohľadu na ich veľkosť.
Už samotné ochorenie familiárnej hypercholesterolémie (FH) preukazuje dostatočným spôsobom kauzálnu úlohu LDL-C pri ateroskleróze. FH je genetický stav, pri ktorom dochádza k strate funkcie LDL-receptora, ktorý je zodpovedný za vychytávanie cholesterolu z LDL do buniek a von z obehu. Pri strate takejto funkcie sa hladiny LDL-C exponenciálne zvyšujú, čo vedie k predčasnej ateroskleróze a ak sa nelieči, aj k skorej úmrtnosti na KVO. FH poskytuje dôkaz, že expozícia LDL-C od raného veku vedie k ateroskleróze a rozsah súvisí s veľkosťou tejto expozície.
ℹ️ Vysoká hladina "zlého" cholesterolu LDL-C v krvi počas dlhého obdobia nášho života významne prispieva k vzniku upchávania tepien (aterosklerózy), čo potvrdili mnohé štúdie.
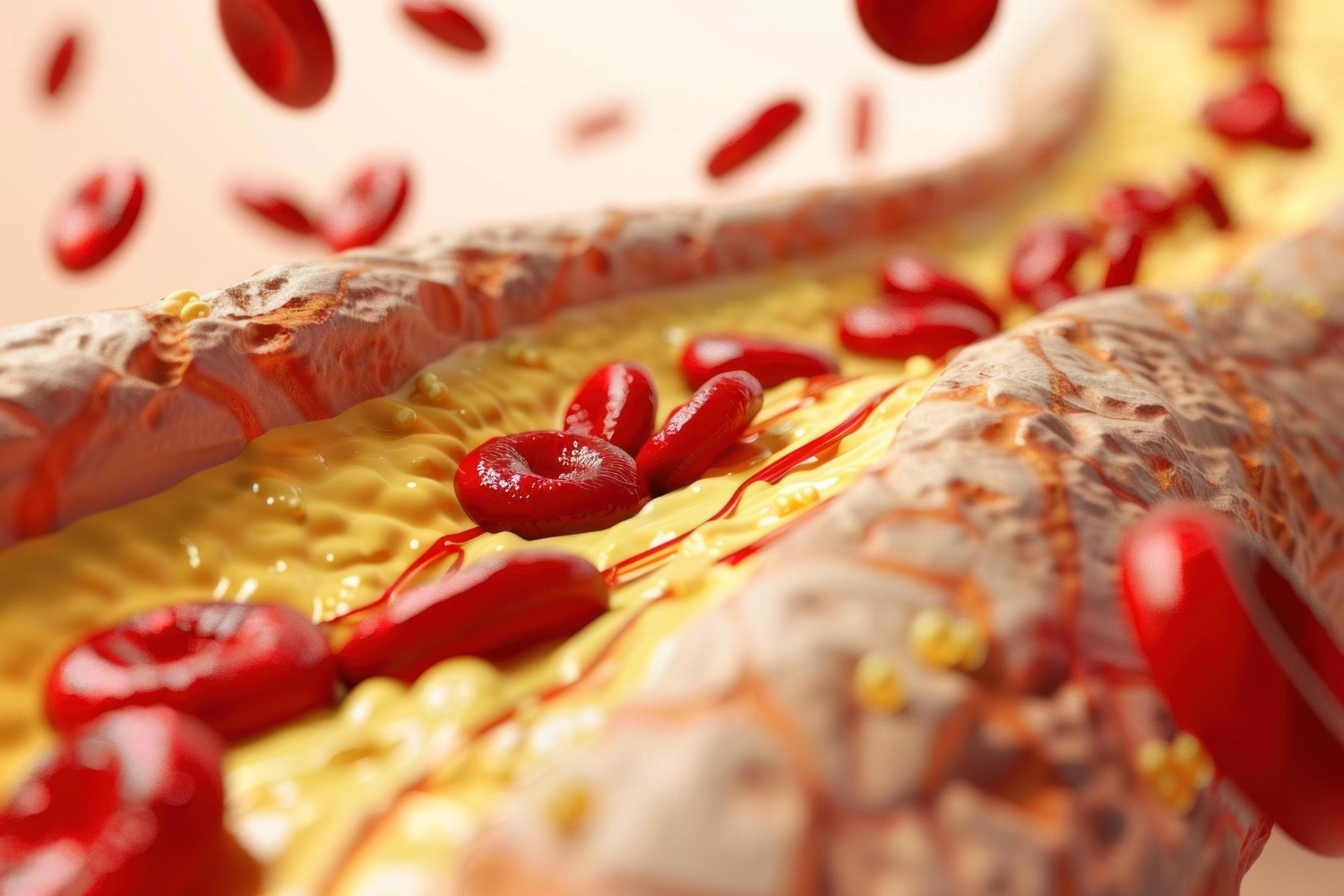
Najprv je dôležité zdôrazniť, že:
1️⃣ LDL-P predstavuje počet častíc LDL v obehu, zatiaľ čo LDL-C je miera obsahu cholesterolu v týchto časticiach.
2️⃣ Všetky lipoproteíny majú okolo seba obalenú proteínovú štruktúru, ktorá sa nazýva apolipoproteín.
Existujú rôzne typy (a podtypy) apolipoproteínov. Každý z lipoproteínov, ktoré sú aterogénne (LDL, Lp(a), IDL, VLDL a CM), má k nim pripojený apolipoproteín B (tzv. apoB). Takže ApoB poskytuje meranie skutočného počtu častíc pre všetky také aterogénne lipoproteíny.
Pre hlbšie dovysvetlenie. Apolipoproteín B (apoB) sa vyskytuje v dvoch izoformách, apoB100 a apoB48. ApoB100 je hlavný štrukturálny apolipoproteín lipoproteínov s nízkou hustotou (LDL) a je prítomná len jedna molekula ApoB100 na časticu LDL. ApoB100 je produkovaný hlavne pečeňou, kde je nevyhnutný pre syntézu a sekréciu lipoproteínov veľmi nízkej hustoty (VLDL) bohatých na triglyceridy. ApoB48 je nevyhnutný pre syntézu a sekréciu chylomikrónov bohatých na triglyceridy, ktoré zohrávajú kľúčovú úlohu pri črevnej absorpcii tukov a vitamínov rozpustných v tukoch.
Za ideálnych okolností Európska spoločnosť pre aterosklerózu odporučila v roku 2019 priame meranie ApoB, keďže poskytuje ďalší nástroj pre podrobnejšie hodnotenie rizika. Neznamená to, že „tradičné“ merania LDL-C a výpočet z neho non-HDL-C nemajú relevanciu. Dôležitým rozdielom medzi meraním non-HDL-C a ApoB je, že zatiaľ čo non-HDL-C poskytuje mieru koncentrácie cholesterolu vo všetkých aterogénnych lipoproteínoch (t. j. cholesterol obsiahnutý vo všetkých lipoproteínoch okrem HDL), ApoB je mierou počtu lipoproteínových častíc. To odráža rozdiel medzi LDL-C a LDL-P. Ak ťa zaujímajú tvoje hodnoty, cena takéhoto merania ApoB je okolo 8-9 eur.
ℹ️ Meranie hodnoty ApoB, ktoré ukazuje počet všetkých škodlivých (aterogénnych) častíc v krvi, je považované za najpresnejší spôsob, ako zistiť, či naozaj tvoj cholesterol je na tom zle.
HDL-C
Ešte sa na chvíľu opäť pristavíme pri HDL. V epidemiológii sú totiž jeho vysoké hladiny spojené s nižším rizikom s srdcovo cievnych a kardiovaskulárnych ochorení. Táto skutočnosť vyvoláva samozrejme záujem o HDL. Veď to je ten dobrý cholesterol, ktorý nie je proaterogenny však? Nuž treba poznamenať, že medikamentózne zvýšenie HDL-C neprinieslo žiadny benefit pre zníženie rizika spomenutých rizík.
Niektorí argumentujú tým, že pri zvýšených hladinách LDL-C so súbežným zvýšením hladín HDL-C nie je zvýšenie LDL-C problémom. Na druhej strane existujú dôkazy, ktoré naznačujú, že HDL-C v skutočnosti sleduje LDL-C. Zvýšenie HDL-C v tomto kontexte je teda kompenzačnou reakciou na zvýšenie LDL-C. Zvýšenie LDL-C zostáva však vzhľadom na už v článku vyššie uvedené stále problematické.
ℹ️ Snaha o zvýšenie HDL bez súčasného zníženia LDL zrejme nepomôže.
Remodelácia lipoproteínov
Ako už nadpis naznačuje, problémom nebude už spomenuté množstvo LDL-C resp. LDL-P, ale aj schopnosť určitých častíc sa zmeniť. Remodelácia lipoproteínov (tzv. Lipoprotein Remodelling) sa týka zmeny veľkosti, hustoty a zloženia lipoproteínov (napr. HDL, LDL, VLDL) v reakcii na metabolické podmienky. Tento proces hrá dôležitú úlohu pri udržiavaní rovnováhy lipidov v tele a je často spojený s rozvojom aterosklerózy, najmä keď dochádza k zvýšeniu hladiny triglyceridov.
Zopakujme si. Lipoproteíny sú častice, ktoré transportujú lipidy (napr. triglyceridy a cholesterol) v krvi. Skladajú sa z lipidového jadra obklopeného vrstvou bielkovín (apolipoproteíny). Hustota lipoproteínov je daná pomerom lipidov k bielkovinám. Vysoká hustota teda znamená viac bielkovín a menej lipidov, kým nízka hustota znamená viac lipidov a menej bielkovín. Keď sa cirkulujúce triglyceridy (TGs) zvýšia nad určitú hranicu, môže to ovplyvniť schopnosť lipoproteínov udržiavať normálny výmenný proces medzi HDL, LDL a VLDL. Tento proces je sprostredkovaný cholesterol-ester transfer proteínom (CETP), ktorý umožňuje výmenu triglyceridov za cholesterol medzi týmito časticami.
A aká je táto hranica triglyceridov pre remodeláciu lipoproteínov? Keď hladina triglyceridov v krvi prekročí 1,5-1,6 mmol/L, dochádza k narušeniu normálneho výmenného procesu medzi lipoproteínmi. Pri tejto hranici:
1️⃣ VLDL začne zahlcovať HDL a LDL prílišným množstvom triglyceridov.
2️⃣ HDL častice sa zmenšujú a remodelujú na menšie a hustejšie subčastice, ktoré sú menej efektívne v odstraňovaní cholesterolu z periférnych tkanív a jeho transportovaní späť do pečene (proces známy ako reverzný transport cholesterolu). Tieto malé husté HDL subčastice sú tiež rýchlejšie katabolizované v pečeni, čo vedie k poklesu cirkulujúcich hladín HDL.
3️⃣ LDL častice sa tiež zmenšujú a stávajú sa hustejšími. Menšie, husté LDL subčastice sú menej efektívne rozpoznávané LDL receptorom v pečeni, čo predlžuje ich prítomnosť v krvnom obehu. Tento predĺžený čas v obehu zvyšuje riziko, že LDL vstúpi do arteriálnej steny, čím sa zvýši riziko vzniku aterosklerózy.
ℹ️ Remodelácia lipoproteínov, teda zmena ich veľkosti, hustoty a zloženia, nastáva pri vysokých hladinách triglyceridov v krvi, a to nad hranicou 1,5-1,6 mmol/L.
Ako celú problematiku dotvárajú tzv. Mendelovské randomizované (MR) štúdie?
Tieto MR štúdie v podstate umožňujú randomizovanú kontrolovanú štúdiu (RTC) počas dlhého obdobia. V mnohých ohľadoch je MR prísnejšie kontrolovaná ako tradičné RCT. Stručne povedané, štúdie MR využívajú našu genetickú diverzitu a polymorfizmy (Polymorfizmus je označenie pre stav, kedy v populácii existujú pre určitý znak minimálne 2 genetické varianty (alely)). Rôzne podskupiny našej populácie budú mať genetické polymorfizmy, ktoré spôsobia, že budú mať prirodzene vyššie alebo nižšie hladiny LDL, zatiaľ čo ostatné krvné lipidy zostanú nedotknuté. Ich stratifikáciou do týchto rôznych skupín a pohľadom na výskyt KVO môžeme určiť, či LDL je alebo nie je kauzálny faktor. Je to teda akoby celoživotná RCT, kde sú ľudia vystavení rôznym hladinám LDL na základe ich genetických rozdielov.
Prakticky vo všetkých štúdiách MR existuje lineárny vzťah medzi hladinami LDL v krvi a výskytom KVO, čo naznačuje kauzálny vzťah. Zníženie výskytu KVO z nízkych hladín LDL bolo väčšie, ako sa predpokladalo. Tento účinok LDL na KVO platí aj pri meniacich sa hladinách HDL, TAG a zápaloch. Napríklad pri vysokej alebo nízkej úrovni zápalu majú ľudia s nižším LDL cholesterolom aj nižšie riziko KVO v porovnaní s ľuďmi s vyššími hladinami LDL.
Mendelovské randomizované štúdie teda poskytujú robustné dôkazy o kauzálnej úlohe LDL-C pri vzniku kardiovaskulárnych ochorení. Výsledky ukazujú, že zníženie LDL-C má jasný prínos pre zníženie rizika KVO, bez ohľadu na ďalšie lipidové a zápalové parametre.
ℹ️ Mendelovské randomizované štúdie poskytujú presvedčivé dôkazy, že zníženie hladiny LDL-C priamo znižuje riziko kardiovaskulárnych ochorení (KVO), a to nezávisle od ostatných faktorov.
🔁 Zhrnutie prvej časti článku
1️⃣ Častice VLDL, IDL, LDL a Lp(a) sa považujú za proaterogénne, čo znamená, že podporujú rozvoj aterosklerózy.
2️⃣ Výskum jednoznačne potvrdil, že LDL cholesterol zohráva kauzálnu úlohu v rozvoji aterosklerózy a kardiovaskulárnych ochorení (KVO), a to nad rámec "iba hypotézy".
3️⃣ V populárnej aj vedeckej literatúre objavujú pokusy znížiť negatívny dopad LDL cholesterolu. Najmä s poukázaním na ľudí s nízkymi hladinami TG, vysokým LDL-C a zároveň aj vysokým HDL-C. Treba však uviesť, že zvýšená záťaž prostredníctvom aterogénnych lipoproteínov, je aj v takomto scenári stále dostatočná na to, aby zapríčinila aterosklerózu.
4️⃣ Epidemiologické štúdie preukázali, že vysoké hladiny HDL-C môžu byť ochranné. Prínos zvyšovania HDL-C v rámci priamych intervencií však nebol potvrdený.
5️⃣ Vysoké hladiny TG sú síce silne spájané s KVO, no po úprave o non-HDL cholesterol toto spojenie už nie je tak evidentné. To naznačuje, že za aterosklerózu sú zodpovedné lipoproteíny obohatené o triglyceridy, a nie však samotné TG. Dokazuje to aj fakt, že veľmi vysoké hladiny TG samy osebe nevedú k ateroskleróze, pretože veľké častice, ako sú chylomikróny a veľké VLDL, nemôžu preniknúť do arteriálnych stien.
6️⃣ Pozornosť si zasluhujú aj zvyškové lipoproteíny, najmä chylomikrónové a VLDL zvyšky, ktoré môžu výrazne vzrásť pri kombinácii vysokého celkového cholesterolu a vysokých TG. Ich úloha v rozvoji aterosklerózy však zatiaľ nie je úplne objasnená.